Jaký je životní cyklus léku?
Životní cyklus léku zahrnuje nejen klinické hodnocení a registraci, patří sem i sledování jeho bezpečnosti po celou dobu výskytu na trhu, případně jeho stažení z trhu s ohledem na závažné nežádoucí účinky.
Uvedení léku na trh předchází dlouholetý vývoj - klinické hodnocení, které probíhá v několika fázích. Výsledkem klinického hodnocení je stanovení nejvhodnějšího dávkování pro pacienta, kdy je lék účinný s minimálním rizikem nežádoucích účinků.
Další etapou je registrace lékovou agenturou (SÚKL nebo EMA), kdy jsou posuzovány předložené výsledky klinického hodnocení a další požadavky zákona týkající se např. kvality zpracovávaných surovin, zajištění správné výrobní praxe a další.
Po registraci může být lék uveden na trh. V té chvíli začíná jeho hodnocení v praxi. Sleduje se výskyt nežádoucích účinků, interakce s dalšími léky a další údaje, které se neprojevily v průběhu provedeného klinického hodnocení.
V případě výskytu neočekávaných nežádoucích účinků je tato informace zpracována a uvedena v souhrnné informaci o léku. Pokud se projeví závažnější nežádoucí účinky, může být lék úplně stažen z trhu.
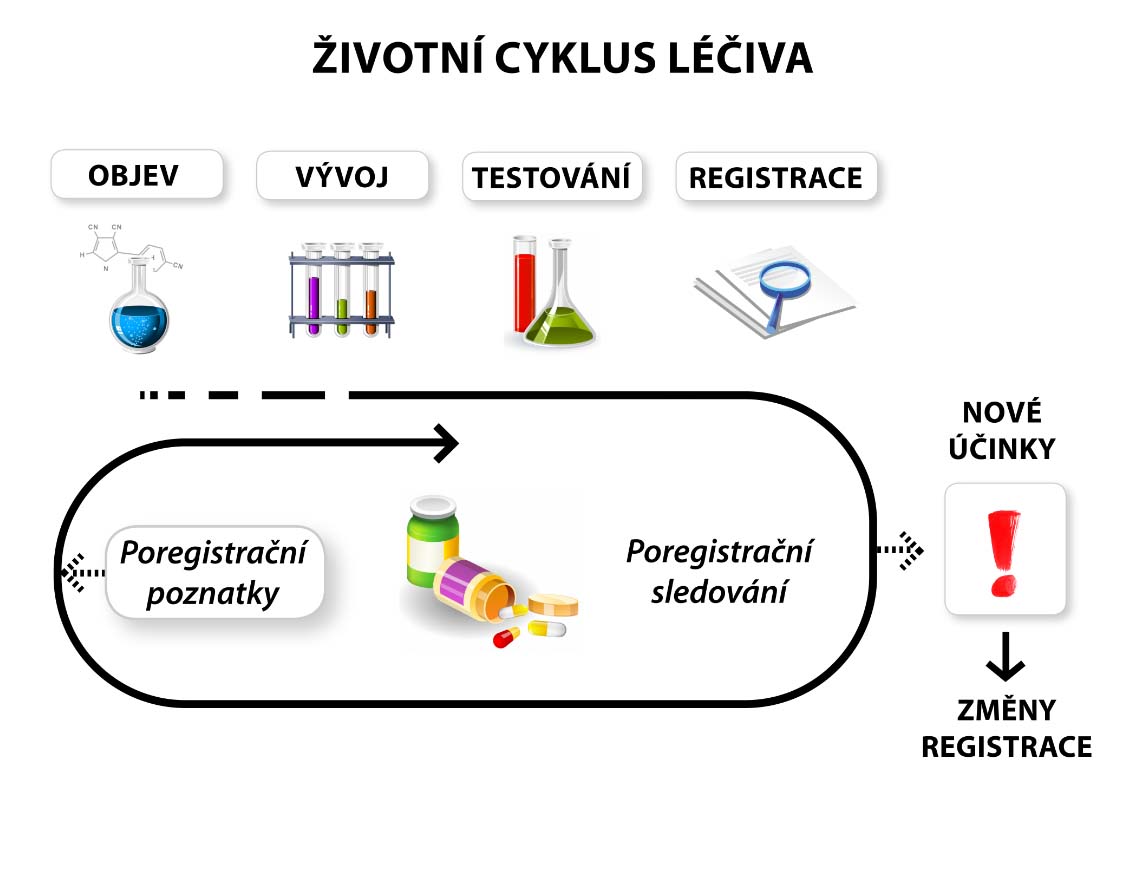
Životní cyklus léku jednoduše popisuje i následující obrázek: